Joaquim Cabot y Boix nació en Barcelona en 1916. Fue médico traumatólogo y jugador de hockey. Como jugador de hockey fue olímpico con la selección española en numerosas ocasiones y participó en varios juegos olímpicos.
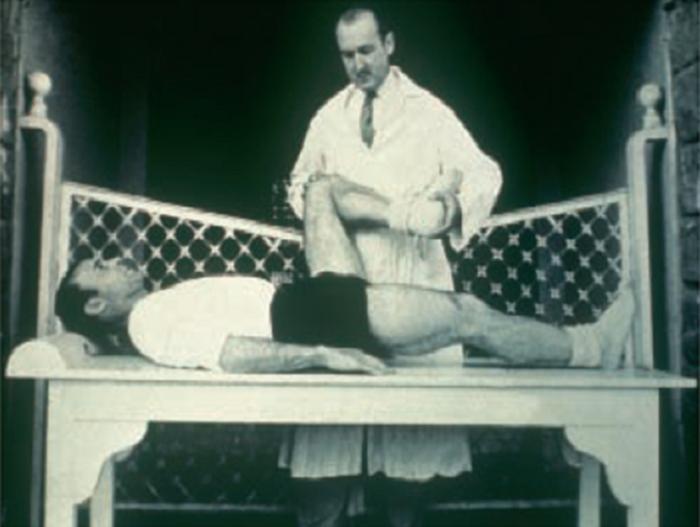
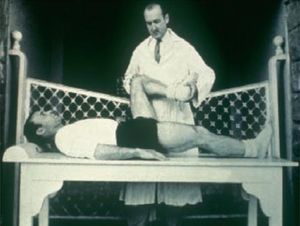
Estudió medicina y cirugía en la Universidad de Barcelona. Se formó en cirugía ortopédica y traumatología en el Hospital Clínico de Barcelona. Se especializó en traumatología del deporte siendo uno de sus pioneros. Fue el director de la Mutualidad de Futbolistas Españoles y en los años 50 fue el médico del FC Barcelona y de la selección nacional española (Figura 1).
Figura 1. El Dr. Cabot explorando la rodilla al mítico César Rodríguez, del FC Barcelona.
Su tesis doctoral (1951) estuvo dedicada a las lesiones meniscales en los deportistas. Fue jefe de servicio del Hospital Clínico y profesor adjunto en la cátedra de cirugía general del profesor Piulachs. Sin lugar a dudas, la figura del Dr. Cabot es capital para entender la extraordinaria tradición que Cataluña tiene en la traumatología del deporte. Murió en 1979.
En 1965, Joaquim Cabot publicó el artículo “Lesiones del músculo en el deporte” en la revista Apuntes de Medicina Deportiva (http://www.apunts.org/es/vol-1-num-005/sumario/13004503/). Con este artículo que hoy presentamos queremos rendir un homenaje al que fue un personaje trascendental para la historia de la medicina y la traumatología del deporte en Cataluña y en España.
IntroducciónEl sistema músculo-esquelético está formado por tejido muscular esquelético, tejido conectivo, tejido nervioso y vasos sanguíneos. Todos estos elementos se disponen y relacionan entre sí y dan lugar a una configuración estructural histológica y fisiológica muy característica determinada por la función del músculo esquelético: la contracción, que determina el alto grado de organización que se observa en sus diferentes niveles tisular, celular y molecular1, 2, 3, 4.
Al ser un tejido tremendamente dinámico, su estructura es vulnerable a la lesión especialmente en el ámbito deportivo, donde supone el tipo de lesión más frecuente con un índice del 31% del total de lesiones y un 30% de relesiones5. Dada la gran variedad de grupos musculares y los múltiples factores que influyen en la lesión, el tiempo de recuperación de estas lesiones es muy variable, incluso en lesiones que se producen en el mismo músculo o grupo muscular6.
En el momento actual, se considera que el conocimiento exacto de los distintos tipos de lesiones, en función de su localización y de sus características, permite poder individualizar de manera más adecuada los tratamientos y, por tanto, conseguir un retorno a la competición más rápido y seguro.
Lesiones musculares agudasLas lesiones musculares agudas son, evidentemente, las que se ocasionan en el ámbito deportivo. Recientemente se han propuesto diversas clasificaciones de la lesión muscular que deben entenderse como complementarias entre sí y que resultan de gran ayuda para comprender la dimensión de las distintas lesiones y su pronóstico6, 7, 8.
Si se pretende resumir la clasificación de la lesión muscular se puede empezar por su primera división básica que es en función de su mecanismo de producción. De esta manera clasificamos las lesiones en lesiones musculares por mecanismo directo (por contusiones más o menos importantes), lesiones musculares por mecanismo indirecto o estiramiento (generalmente excéntrico) y el dolor muscular de inicio retardado (Tabla 1)4. Es importante destacar también las entidades denominadas como desórdenes funcionales musculares como pueden ser las alteraciones neuromusculares o las microrroturas no visibles mediante pruebas de imagen pero que pueden provocar dolor y pérdida de días de actividad deportiva8.
Tabla 1. Clasificación de las lesiones musculares en función del mecanismo de producción
| Mecanismo de producción |
| Directo (según clínica) |
| Grado 1. Arco de movilidad conservado |
| Grado 2. Arco de movilidad limitado < 50% |
| Grado 3. Arco de movilidad limitado > 50% |
| Indirecto (según ecografía o RM) |
| Grado 0. Antecedente lesión: no concreto. Exploración física: anodina. Imagen: negativa |
| Grado 1. Antecedente lesión: no concreto. Exploración física: anodina. Imagen: edema |
| Grado 2. Antecedente lesión: concreto. Exploración física: específica. Imagen: disrupción muscular |
| Grado 3. Antecedente lesión: concreto y brutal. Exploración física: aparatosa o imposible. Imagen: rotura muscular o avulsión |
| Dolor muscular postesfuerzo |
| De agujetas a rabdomiólisis |
Una segunda división a tener en cuenta es la clasificación de la lesión muscular en función de la zona anatómica afectada. Para comprender correctamente esta división es preciso conocer que el aparato locomotor posee un componente fascial y un componente músculo-tendinoso. El componente fascial es estructural y está formado por elementos conectivos (epimisio, perimisio y endomisio). El componente músculo-tendinoso es funcional y dinámico y lo forman los tendones y las aponeurosis como transmisores de fuerza, y la fibra muscular como elemento contráctil.
Esta división toma un especial interés en las lesiones por mecanismo indirecto. Este tipo de lesión suele afectar a músculos poliarticulares del esqueleto apendicular y, habitualmente, se deben a una contracción excéntrica. Así pues, una lesión se puede situar en la unión tendoperióstica, en el componente músculo-tendinoso (unión músculo-tendinosa) o en el componente miofascial (unión miofascial), siendo las de peor pronóstico las músculo-tendinosas (Tabla 2).
Tabla 2. Clasificación de las lesiones musculares en función de la región anatómica afectada
| Componente tendinoperióstico |
| Avulsión desinserción |
| Componente músculo-tendinoso (o músculo aponeurótico) |
| Expansión aponeurótica periférica: lesión músculo-tendinosa |
| Aponeurosis central: lesión del tendón o aponeurosis central |
| Componente miofascial |
| Lesión miofascial |
Dejando de lado las lesiones musculares por mecanismo directo y centrando el estudio en las provocadas por un mecanismo indirecto, es importante resaltar que suelen producirse muy cerca de la unión músculo-tendinosa, donde la capacidad de estiramiento (elasticidad) sin rotura no es tan grande como en el vientre muscular, debido a su particular histología, y en la que las líneas Z de las fibras musculares se funden con las fibras tendinosas. Es, por tanto, la región más débil de la cadena hueso-tendón-músculo9.
Estas lesiones son producidas habitualmente por un ejercicio intenso con gran componente de trabajo negativo (excéntrico). Este tipo de trabajo produce tensiones excesivas que acaban dañando la estructura a nivel celular. Pueden observarse alteraciones en las bandas Z sacoméricas y cambios proteicos en las células musculares, disrupción miofibrilar y alteraciones sanguíneas locales. Las manifestaciones clínicas son el dolor, la pérdida inmediata o retardada de fuerza, la disminución del rango de movimiento, el edema y la pérdida de capacidad de control motor en forma de déficits propioceptivos.
Los músculos poliarticulares son más propensos a las lesiones ya que son músculos relacionados con la movilidad en 2 articulaciones y dependen, por tanto, de la posición de ambas. Asimismo, controlan el movimiento articular producido por el grupo antagonista, lo que hace que las lesiones sean mucho más frecuentes en disciplinas deportivas que requieran aceleraciones rápidas o esfuerzos explosivos. Un alto porcentaje de fibras rápidas de tipo II en estos grupos musculares es otro factor de susceptibilidad, debido a su mayor fatigabilidad.
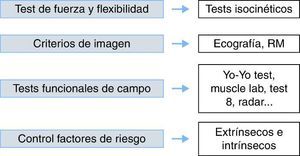
Factores de riesgo (causas predisponentes)Uno de los principales condicionantes a tener en cuenta respecto a las lesiones musculares en el momento actual es el conocimiento de las causas predisponentes o factores de riesgo. Es precisamente la suma de estos factores de riesgo más un acontecimiento desencadenante lo que acaba produciendo la lesión muscular. Por este motivo, el control de estos factores puede suponer una disminución muy importante de la incidencia lesional.
Los factores de riesgo pueden clasificarse en intrínsecos (propios del individuo) y extrínsecos (Tabla 3).
Tabla 3. Factores de riesgo intrínsecos y extrínsecos que condicionan el riesgo de lesión muscular
| Factores de riesgo intrínsecos | Factores de riesgo extrínsecos |
| Edad | Errores de entrenamiento |
| Sexo | Material utilizado |
| Composición corporal | Condiciones ambientales |
| Predisposición genética | Condicionantes psicológicos |
| Historial previo de lesiones | Momento de la temporada |
| Estado de salud general | Hábitos tóxicos |
Otros factores de riesgo a tener en cuenta son las alteraciones de los ejes mecánicos de las extremidades, un apoyo irregular en la pisada, el estado del balance muscular y de la coordinación, la fatigabilidad muscular y el grado de elasticidad10.
Las alteraciones de los ejes mecánicos de las extremidades o un apoyo irregular suelen conducir a un desequilibrio del balance muscular y de la coordinación que contribuye a generar una debilidad muscular que provoca que el músculo tenga una menor capacidad de resistencia a la tensión y que, por tanto, pueda romperse más fácilmente11.
La fatiga muscular produce una disminución de la capacidad de absorber energía (amortiguación) y de generar tensión en la contracción excéntrica, a pesar de que se mantiene sin alteraciones la capacidad de alargamiento del músculo hasta el momento en que se produce lesión. Es decir, el músculo fatigado debe estirarse más para ejercer la misma acción amortiguadora.
El déficit de elasticidad se relaciona básicamente con lesiones recidivantes. La alteración de las propiedades viscoelásticas de un músculo produce una disminución de la capacidad de soportar tensión para una misma carga de tracción mantenida que se traduce en una disminución de la resistencia de este músculo. El estiramiento y los ejercicios de flexibilidad, además de tener efectos a nivel neuromuscular, cambian las propiedades biomecánicas del músculo sometido a tensión. En este mismo sentido, el calentamiento muscular (ya sea mediante ejercicio o por métodos físicos) aumenta la capacidad de estiramiento muscular por tensión y su capacidad de realizar fuerza de contracción.
Frecuencia y localización de las lesionesLa frecuencia y localización de las diferentes lesiones dependen de múltiples factores. Entre ellos destacan principalmente los factores de riesgo comentados previamente. En términos generales, la frecuencia puede estimarse en un 31% de todas las lesiones observadas en el deporte y el índice de recaídas se estima entre un 14-32% en función del tipo de deporte.
En cuanto a la localización, la extremidad inferior y, de manera más concreta, el muslo es donde asientan el mayor número de lesiones debido a los grandes grupos musculares que existen en esta región y a sus particulares características. Sin duda alguna, el grupo más afectado es el grupo isquiosural, seguido del cuádriceps; posteriormente, en función de las series estudiadas, se encuentran la región muscular aductora y la región posterior de la pierna (calf muscles)4, 6, 8, 12, 13, 14, 15, 16, 17.
Evolución anatomopatológica del desgarro muscularExiste cada vez un mayor interés en el conocimiento de la evolución anatomopatológica de la lesión muscular ya que muchos de los tratamientos de reciente aparición se basan en el profundo conocimiento de este proceso.
Una de las características principales del tejido muscular es que se trata de un tejido dinámico que interacciona con el medio que lo rodea y que es capaz de reaccionar a los estímulos externos. Todo ello permite que sea manipulable externamente tanto por procedimientos físicos (masajes, campos magnéticos...) como por procedimientos químicos (AINE, antifibróticos…).
A nivel biológico, el tejido muscular esquelético es una fuente importante de distintos tipos de células madre somáticas, células madres miogénicas entre las que se incluyen las células satélites que son las principales responsables del crecimiento muscular y la regeneración muscular y células madre multipotentes derivadas del músculo.
El potencial regenerativo del músculo disminuye con la edad y se asocia a un incremento de la aparición de la fibrosis. Actualmente se sabe que la cronología de la reparación de la lesión muscular no es uniforme ni homogénea en el tiempo. La importancia de un determinado factor de crecimiento y su repercusión biológica varían y se modifican a lo largo del tiempo, de igual manera que la cantidad e intensidad de determinadas reacciones biológicas.
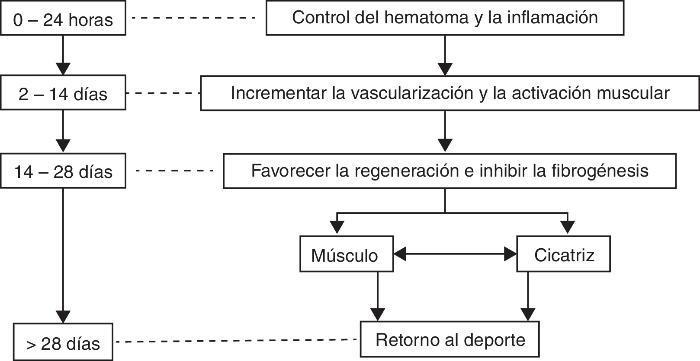
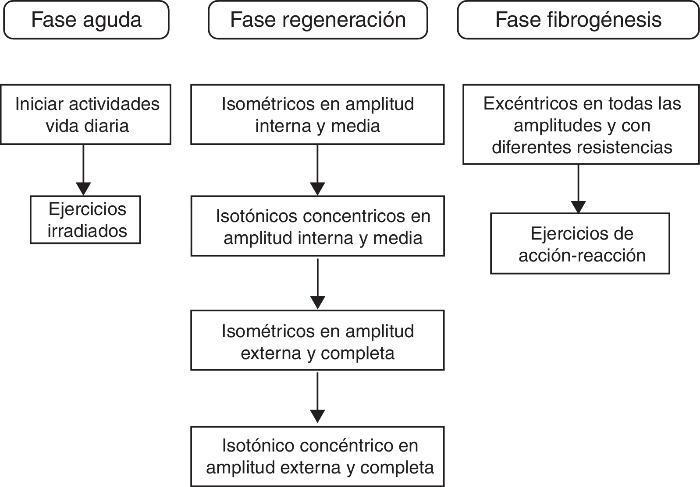
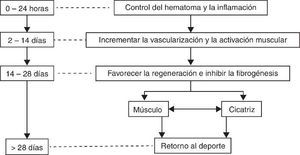
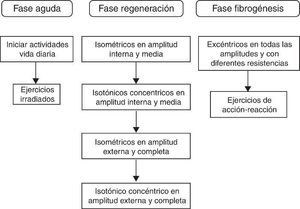
El tratamiento se establece en 3 fases fundamentales a contar desde el día de la producción de la lesión muscular. La primera fase de lesión aguda corresponde al periodo comprendido desde el instante de la producción de la lesión hasta las primeras 24 o 48 h. La segunda fase de regeneración se extiende entre las primeras 24 h y los 14 días desde la lesión, y la tercera fase de fibrogénesis desde la segunda semana hasta la cuarta semana (Figura 2).
Figura 2. Objetivos del tratamiento en función de la fase de reparación muscular.Fuente: adaptada de Balius 4 .
Fase agudaDurante las primeras 24-48 h tras una lesión muscular se produce hematoma por extravasación de sangre de los vasos sanguíneos rotos, inflamación, liberación de citocinas que van a activar las células satélites y de fibroblastos, estimulación de macrófagos, neutrófilos y linfocitos. El reclutamiento de macrófagos que se produce provoca el inicio de los fenómenos degenerativos. La inflamación va a producir degeneración fibrilar de las proteínas miofibrilares, la actina y miosina, que son los objetivos fundamentales de la degeneración fibrilar y celular. La vasodilatación y la angiogénesis son promovidas por el platelet-derived growth factor-D (PDGF-D) y por el vascular endothelial growth factor-E (VEGF-E)4, 18, 19.
Se considera básico, para una buena respuesta biológica, el aumento de la vascularización en la zona de lesión, la mejora del estado metabólico celular y el incremento del suministro de oxígeno en el lugar de la lesión.
Fase de regeneraciónEn esta fase es fundamental la activación y estimulación de las células satélites musculares por la mediación de los factores de crecimiento y otras sustancias químicas. Destaca por su efecto mediador el fibroblast growth factor basic (bFGF or FGF-2), que es un componente básico en la cascada de la regeneración muscular, además, al igual que el PDGF-B, es un componente importante para promover la arteriogénesis y miogénesis en el músculo dañado19, 20.
La diferenciación de las células satélites depende de los distintos factores de crecimiento20. Pueden diferenciarse en 3 líneas celulares fundamentalmente: fibroblastos, que en el lugar de la lesión se sumarán a otros fibroblastos que proceden de otras zonas del organismo; miofibroblastos, células situadas entre la fibra muscular y el fibroblasto; o mioblastos, precursores de la fibra muscular propiamente dicha. Este punto tiene una importancia crucial ya que, dependiendo del tratamiento aplicado, es posible favorecer una reparación fibrótica (fibrosis o cicatriz) o una regeneración muscular.
Mención especial requiere el transforming growth factor-beta 1 (TGF-beta 1) por su implicación en la generación de fibrosis21. El TGF-beta 1 es un potente inductor de la síntesis de colágeno, productor de citocinas y transdiferenciación de miofibroblastos implicados en la fibrosis. Aumenta la proliferación de fibroblastos, la migración, adhesión y formación de la matriz extracelular. Asimismo, es primordial para la transformación de la célula satélite en fibroblasto y, en menor medida, en miofibroblasto; de aquí se deduce la necesidad del bloqueo de este factor.
Fase de fibrogénesisEn esta fase (14-28 días) se produce mayor actividad celular en todas las líneas celulares comentadas y disminuye la diferenciación de las células. Algunos agentes terapéuticos han mostrado la capacidad de inhibir la fibrogénesis y mejorar la regeneración muscular por medio de la inhibición del TGF-beta 1 (decorina, relaxina, cucurmina, suramina, gammainterferón…) aunque muchos de ellos se encuentran todavía en fase de estudio.
La inhibición de la fibrogénesis lo que realmente permite es disponer de más tiempo para permitir la correcta diferenciación de las células precursoras de la fibra muscular.
Sintomatología, diagnóstico y pronósticoEl conocimiento clínico y anatómico es indispensable para la evaluación de una lesión muscular. La anamnesis, la inspección y la palpación ofrecen un diagnóstico inicial de la lesión que posteriormente será confirmado por las diferentes pruebas complementarias de las que se dispone. Esta misma valoración inicial debe permitir poder establecer un pronóstico de esta lesión en función de su gravedad.
SintomatologíaVariará siempre en función de la gravedad de la lesión. Así pues, en las lesiones de 1.er grado existe un traumatismo mínimo que la mayoría de las veces no es recordado por el paciente y únicamente presenta molestias una vez terminada la actividad o a las 24-48 h. En las de 2.° y 3.er grado, la sintomatología se inicia, generalmente, con motivo de un impulso, una aceleración brusca, un sprint, un chut o un cambio de ritmo22. Por tanto, el paciente recuerda perfectamente el momento de la lesión y lo puede llegar a definir como un dolor agudo punzante o como una «pedrada». En caso de contusión, si el golpe directo se ha producido sobre un músculo en contracción, la lesión siempre será de peor pronóstico que si el músculo se encuentra relajado.
Diagnóstico clínicoEn lesiones musculares de 1.er grado, la inspección prácticamente no aporta información. En algunos casos de contracturas, delayed onset muscle soreness (DOMS) o rabdomiólisis de esfuerzo de músculos superficiales, es posible observar aumento de tono y grosor muscular.
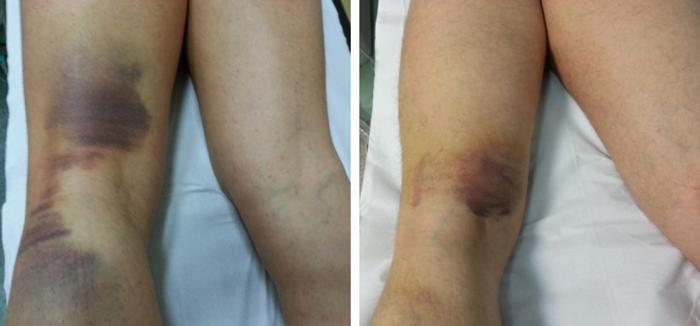
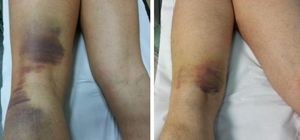
Las lesiones musculares de grado 2 y 3 pueden tener una inspección inmediata negativa, pero con el tiempo (horas o días en función del grado) es posible observar una tumefacción, que afecta al músculo lesionado, secundaria al hematoma o al edema reactivo. Posteriormente, suele aparecer una sufusión hemática cutánea de extensión variable y distal a la lesión (Figura 3).
Figura 3. Sufusión hemática típica de las lesiones de la musculatura isquiosural.
En las lesiones de grado más elevado, la inspección permite descubrir inicialmente un tumor visible, junto a un hachazo, que se hace más evidente durante la contracción (muñón muscular) y que suele quedar como secuela sin que esto comprometa la función. Este muñón muscular, que aparece en contracción y desaparece en relajación, no debe confundirse con una hernia muscular, que aparece en relajación y desaparece en contracción4.
En cuanto a la palpación se refiere, debería realizarse cuanto antes mejor para no tener la dificultad añadida de la aparición del edema y el posible hematoma. En la palpación debe tenerse en cuenta si existe un hachazo en el relieve muscular, ya que esto implicará una lesión muscular de mayor grado. Otro de los signos a tener en cuenta es la presencia o ausencia de bamboleo muscular ya que cuanto menor sea el bamboleo muscular existente peor será el pronóstico de la lesión.
La movilidad también es, obviamente, un elemento indispensable para valorar la lesión, ya que cuanto más grave sea la lesión, mayor es la dificultad de realizar movimientos activos (especialmente contrarresistencia) y mayores también la disminución de la movilidad de las articulaciones vecinas al segmento.
Diagnóstico por imagenEs de todos conocida la gran importancia que tienen actualmente las diferentes pruebas de imagen, en concreto la ecografía y la resonancia magnética (RM), para la valoración de la lesión muscular, especialmente en el mundo del deporte. En los últimos años, la mayor portabilidad y precisión de las sondas de ecografía y la mayor calidad y resolución de las máquinas de RM permiten conocer con una gran exactitud la magnitud, la localización y el pronóstico de las lesiones. A este hecho debe añadirse la capacidad de exploración dinámica que aporta la ecografía muscular.
Tanto la RM como la ecografía permiten un diagnóstico correcto de las lesiones musculares. La ecografía puede ser la primera exploración a realizar pero hay que tener en cuenta que roturas de grado 1, sobrecargas o lesiones en determinados músculos (sóleo o psoas) pueden pasar desapercibidas en ecografía con frecuencia23, 24.
Tanto la ecografía como la RM deben ser consideradas técnicas complementarias. La primera tiene la ventaja de ser dinámica y permitir el intervencionismo (punción evacuadora e infiltraciones ecoguiadas) y la segunda, de ser más sensible para detectar edema y permitir una mayor amplitud en el campo de visión.
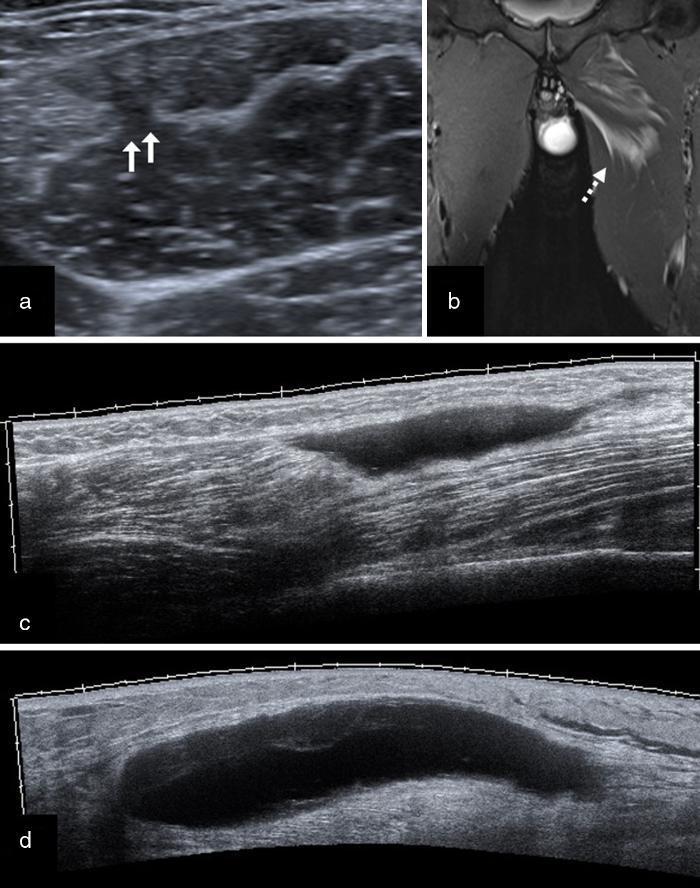
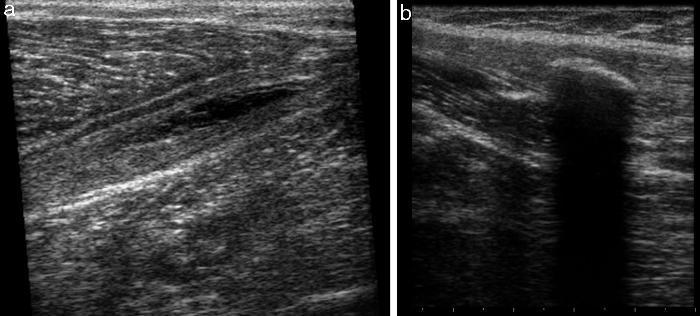
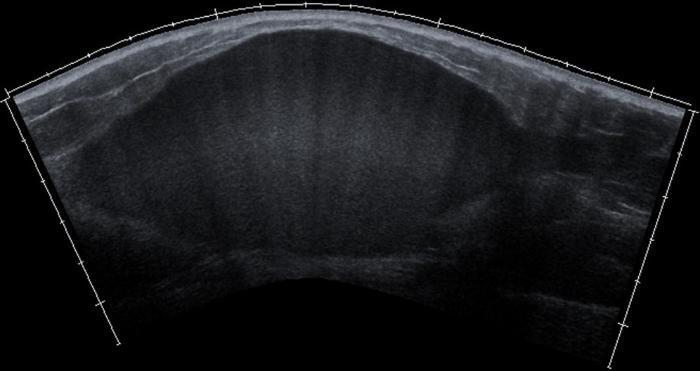
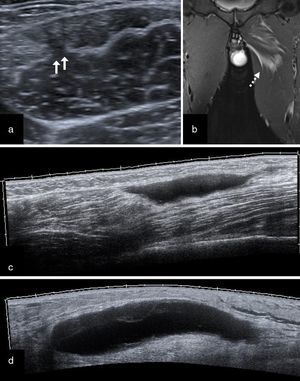
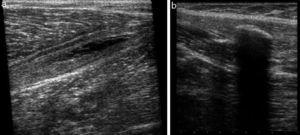
Un hecho muy importante a tener en cuenta es que la ecografía y la RM tienen la capacidad de valorar edema, hemorragia o retracción de fibras, pero no la solución de continuidad (gap) de forma precisa (Figura 4). Esto supone todavía una gran limitación, especialmente a la hora de intentar definir de manera precisa un pronóstico para cada tipo de lesión25, 26.
Figura 4. Imagen de los diferentes grados de lesión muscular. a) Lesión grado 1 proximal músculo-tendinosa del aductor mediano en su parte proximal (flechas). Ecografía en eje corto. b) Misma lesión: RM coronal T2 STIR. c) Lesión grado 2 de la porción larga del bíceps femoral a nivel distal. Ecografía en eje largo (panorámica). d) Lesión grado 3 consistente en rotura completa de la unión músculo-tendinosa distal de la cabeza medial del gastrocnemio (hematoma en tennis leg). Ecografía en eje largo (panorámica).
TratamientoEl tratamiento de las lesiones musculares no sigue un modelo único ni un protocolo concreto. Este tratamiento variará, como se ha comentado anteriormente, en función del tipo de lesión, del músculo afectado, del deportista y de la actividad deportiva que se realice27.
Es posible intentar establecer ciertos elementos o pautas comunes en función de cada una de las fases de la lesión.
Fase agudaEl tratamiento inicial de elección en el momento de producirse la lesión sigue siendo la aplicación de reposo, hielo, compresión y elevación, concocido como RICE (del inglés, rest, ice, compression, elevation). El objetivo principal en la fase aguda es el de reducir la formación del hematoma y que el edema intersticial acorte la isquemia del tejido y se acelere de esta forma la regeneración. Se aconseja un reposo relativo de entre uno y 3 días en función de la gravedad o localización de la lesión4.
La aplicación de hielo, a veces controvertida, minimiza el sangrado inicial en la lesión primaria; es decir, permite controlar la hemorragia y disminuir la lesión tisular secundaria ya que la actividad metabólica y la demanda de oxígeno se reducen. El consumo de oxígeno disminuye de 2 a 5 veces por cada 10 °C que descienda la temperatura. De esta manera, los tejidos vecinos sanos, que sufren una disminución de aporte sanguíneo, no se verán dañados ya que sus necesidades metabólicas disminuyen con la crioterapia.
Los vendajes compresivos de tipo vascular son útiles en esta fase para fomentar el recambio sanguíneo en el foco de la lesión, controlar el hematoma y mejorar el drenaje. Los masajes intensos y profundos están contraindicados por su relación con el aumento de la aparición de calcificaciones musculares por la estimulación de los mecanorreceptores y por el riesgo de agrandar la lesión19. Igualmente, en esta primera fase el estiramiento estará contraindicado ya que el punto de lesión es débil y la solicitación tensil podría agravar la lesión.
Fase de regeneraciónDurante la fase de regeneración, la base del tratamiento es la movilización activa temprana para conseguir que el tejido muscular vuelva a adaptarse a las solicitaciones propias del deporte27.
El trabajo activo durante esta fase mejora, por un lado, la circulación sanguínea, al aportar oxígeno al tejido lesionado y, por otro lado, somete al tejido a unas cargas mecánicas que facilitan la restructuración del colágeno, permitiendo una gran producción de tejido de granulación y cicatricial, así como una orientación paralela en la cicatriz del tejido conectivo.
Esta rehabilitación activa debe aplicarse de manera progresiva y se deben planificar las intervenciones, según el grado, la localización topográfica de la lesión y su evolución. El signo guía desde las fases iniciales debe ser el umbral de la molestia, nunca el del dolor (molestia se entiende como el dolor soportable que no modifica la función).
El estiramiento suele iniciarse entre el 3.er y el 5.° día. Inicialmente se prescriben estiramientos estáticos activos en tensión pasiva, por la acción del antagonista y, a medida que va incrementando la tolerancia y se normaliza el arco de movilidad, se introducen los estiramientos estáticos activos en tensión activa (contracción del agonista).
La progresión de ejercicios se realiza de menor a mayor solicitación de la región afectada (Figura 1).
Fase de fibrogénesisEl objetivo principal de esta fase es el de realizar de nuevo una correcta adaptación del tejido muscular a la actividad deportiva que se le va a solicitar.
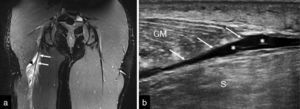
Durante esta fase de readaptación se realizan estiramientos progresivos combinados con trabajo activo (aumento de la intensidad de las contracciones musculares de isométricas a excéntricas) sin dolor (Figura 5).
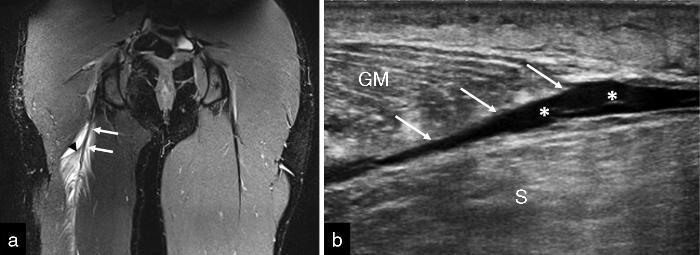
Figura 5. Déficit en la visualización del defecto fibrilar exacto en estudios de RM y ecografía. a) Coronal T2 STIR rotura músculo-tendinosa de la cabeza larga del bíceps femoral que interesa el tendón común (flechas). Se observa retracción de fibras (punta de flecha) y edema intramuscular en pluma (*). No se objetiva defecto fibrilar con exactitud. b) Rotura miofascial de la cabeza medial del gastrocnemio medial (flechas). Estudio ecográfico en eje largo. Se observa retracción de fibras (flechas) y colección líquida miofascial (*), pero no se objetiva con exactitud el defecto fibrilar.GM: gastrocnemio medial. S: sóleo.
¿Cuándo puede el atleta participar de nuevo en competición? El concepto de vuelta a la competiciónFrecuentemente se utiliza la expresión inglesa return to play (RTP) para designar el concepto de vuelta a la competición (VC). El proceso de decisión de VC es uno de los más complejos de la medicina del deporte, porque se trata de decidir cuándo un deportista lesionado o enfermo puede volver de manera segura a la práctica deportiva o a la competición12. El proceso de VC debe individualizarse en cada lesión y siempre en función del tipo de lesión, de la localización, del nivel del deportista y del deporte que practica28.
El momento en que se crea un pronóstico y se determina el proceso del VC se condiciona un riesgo de relesión, es decir, el riesgo de recaída, en la misma temporada o en las temporadas siguientes29. Se considera recidiva cuando la lesión se localiza en la misma región anatómica y con la misma forma de presentación. Si tal recaída sucede antes de los 2 meses de la vuelta a la actividad se considera temprana; tardía si aparece entre los 2 y 12 meses y retardada cuando aparece 12 meses después12.
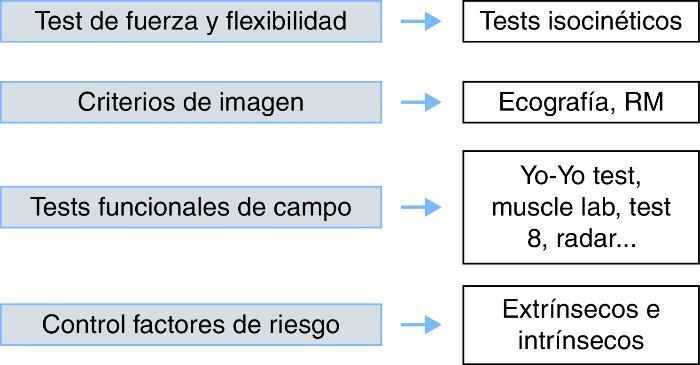
Para poder establecer un tratamiento y un pronóstico encaminado a que el VC sea lo más corto y seguro posible, es necesario conocer el mecanismo y el grado de lesión y su localización exacta. En este sentido, a día de hoy, se dispone de algunos marcadores, factores o pruebas que, con mayor o menor evidencia científica, permiten decidir cuándo una lesión va a tener un mayor tiempo de VC (Figura 6).
Figura 6. Progresión de ejercicios poslesión.Fuente: adaptado de Balius 4 .
Posibles complicaciones de las lesiones muscularesDebido a la gran diversidad de lesiones que existen y a la gran cantidad de factores que pueden influir en las distintas fases de reparación de la lesión, es relativamente frecuente que existan condicionantes que puedan alterar el proceso evolutivo normal de la lesión muscular19, 30. Algunos de ellos son los que se exponen a continuación.
Cicatriz fibrosa y cicatriz cálcicaLa cicatriz fibrosa (Figura 7) consiste en una reparación muscular hipertrófica de tejido fibroso que produce una pérdida de la elasticidad del tejido muscular y que puede provocar dolor durante el esfuerzo y posteriormente a este. En principio, el tratamiento es conservador mediante estiramientos, infiltraciones u ondas de choque. La cirugía se reserva únicamente para casos que no respondan a estos tratamientos.
Figura 7. Tabla-resumen de los criterios de VC.
La cicatriz cálcica (Figura 7) forma parte de la evolución no deseada de una lesión muscular que cicatriza en forma de tejido cálcico y nunca debe confundirse con la miositis osificante que, como se explicará posteriormente, se trata de un proceso metabólico patológico de la propia lesión. Si esta cicatrización altera el funcionamiento del músculo y no puede tratarse de manera conservadora, deberá recurrirse a la cirugía.
HematomasLos hematomas (Figura 8) se forman por la extravasación sanguínea secundaria a la rotura de fibras ya sea por mecanismo directo o indirecto. Siempre que sea posible está indicada su evacuación ya que este hematoma genera un aumento del proceso inflamatorio, del tejido cicatricial y de la pérdida de función muscular. Esta evacuación puede realizarse sin ningún problema de manera percutánea bajo control ecográfico.
Figura 8. a) Imagen de cicatriz fibrosa 3, lesión de la UMT distal de la cabeza medial del gastrocnemio. b) Imagen de cicatriz cálcica 3, lesión miotendinosa proximal del aductor largo.
Los casos en los que el hematoma sea enquistado o no sea posible su drenaje mediante ecografía pueden requerir desbridamiento quirúrgico.
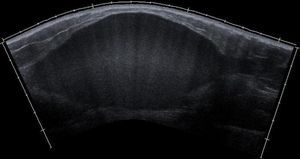
Miositis osificanteSe trata de una formación anormal de hueso laminar maduro dentro de los tejidos blandos esqueléticos donde habitualmente no existe hueso (Figura 9). Su incidencia oscila del 9 al 20% y su patogenia es desconocida, aunque habitualmente se produce de forma secundaria a un traumatismo muscular inicial generalmente en la cara lateral del muslo (músculos vasto lateral y vasto intermedio).
Figura 9. Imagen ecográfica longitudinal panorámica de hematoma intramuscular en glúteo mayor en fase de coagulación.
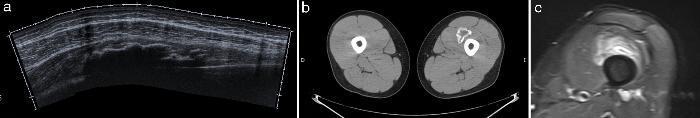
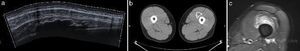
La clave del diagnóstico se encuentra en objetivar osificación periférica en las pruebas de imagen31. Esta osificación periférica es característica de la miositis osificante y la diferencia del osteosarcoma (Figura 10).
Figura 10. Imágenes de miositis osificante. a) Ecografía panorámica en eje largo de vasto intermedio donde se objetiva osificación completa tras una lesión por contusión. b) Corte axial TC que muestra masa osificada en el vasto interno. c) RM axial T2 STIR. Osificación con médula y cortical óseas maduras.
Lo básico en su tratamiento es intentar evitar desde el principio la inmovilización y la artrofibrosis que se dan por la rigidez muscular y articular mantenida32. A nivel farmacológico, el tratamiento de elección es la indometacina. Finalmente, en casos residuales sintomáticos puede recurrirse a la exéresis quirúrgica siempre que hayan pasado un mínimo de 6 meses tras la lesión y la gammagrafía ósea de 3 fases sea negativa.
Síndromes compartimentales (agudos o crónicos)El síndrome compartimental se caracteriza por la elevación de la presión intersticial en un compartimento óseo-fascial cerrado que da lugar a un compromiso vasculonervioso. Este puede ser agudo o crónico, dependiendo de la causa del aumento de la presión y de la duración de los síntomas33.
El síndrome compartimental agudo se basa siempre en la existencia de una agresión previa (fracturas o traumatismos de partes blandas). El síndrome compartimental crónico se relaciona con el esfuerzo físico y es más frecuente en el compartimento anterior o profundo de la pierna y en los antebrazos34.
El diagnóstico es clínico y únicamente puede ser confirmado por la medición directa de la presión intracompartimental35.
El tratamiento consiste en la fasciotomía completa de todos los compartimentos implicados (urgente en el caso del compartimental agudo y programada en el caso del crónico).
ConclusiónHemos presentado el estado de la cuestión de las lesiones musculares en el deporte. Se han expuesto los factores de riesgo, la frecuencia de las lesiones y su localización, así como su evolución anatomopatológica. Igualmente se ha profundizado en el diagnóstico clínico y de imágenes, para finalizar con una valoración de las lesiones musculares.
Sin duda alguna, el Dr. Cabot en el artículo publicado en la revista Apuntes de Medicina Deportiva en 1965 realizó una brillante puesta al día del mismo tipo de lesiones. Es por ello que hemos querido homenajear a un personaje primordial de la medicina del deporte en Catalunya y España.
Recibido 2 Enero 2015
Aceptado 20 Enero 2015
Autor para correspondencia. carlespedret@gmail.com